Uso de inibidores de COX-2 em oncologia veterinária
As cicloxigenases (COX) são enzimas responsáveis pela cicloxigenação e peroxidação do ácido araquidônico presente na membrana celular, levando a formação de prostaglandinas.
Dietas caseiras cozidas
Cuidados essenciais
Cuidados especiais
Dietas caseiras cruas
Dietas caseiras cozidas
Cuidados essenciais
Cuidados especiais
Dietas caseiras cruas

Introdução
As cicloxigenases (COX) são enzimas responsáveis pela cicloxigenação e peroxidação do ácido araquidônico presente na membrana celular, levando a formação de prostaglandinas. A COX, enzima chave que catalisa a biossíntese das prostaglandinas, tem duas isoformas principais, a cicloxigenase-1 (COX-1) e cicloxigenase-2 (COX-2). As duas isoformas são formadas por uma estrutura protéica primária similar, sendo a COX-1 expressa constitutivamente e a COX-2 induzida principalmente em processos inflamatórios e neoplásicos.
Diversos estudos realizados correlacionam o desenvolvimento e progressão de alguns tipos de neoplasias em humanos e animais à presença da COX-2 e a partir destas observações foram sugeridos os benefícios do uso de inibidores de COX-2 na terapia antineoplásica. Pacientes que faziam uso de anti-inflamatórios não esteroidais para alívio da dor devido a tumores gastrointestinais, apresentavam regressão do tumor. Outros estudos mostraram redução de 40 a 50% do risco de desenvolvimento de câncer de cólon e reto em pessoas que usavam regularmente anti-inflamatórios não esteroidais.
MECANISMOS ENVOLVIDOS NA EXPRESSÃO DE COX-2 E CÂNCER
Vários mecanismos foram propostos na tentativa de explicar a relação entre a expressão de COX-2 e consequentemente a superprodução de prostaglandinas pelas células neoplásicas. Dentre estes mecanismos, são citados a inibição da apoptose, a indução de angiogênese, o estímulo à proliferação celular, o aumento na capacidade de invasão tumoral (favorecendo os mecanismos de metástase) e a supressão do sistema imune.
Figura 1 – Mecanismos relacionados a produção de prostaglandinas e o desenvolvimento neoplástico
Sendo assim, a diminuição da apoptose devido à expressão de COX-2 nas células neoplásicas, aumenta a sobrevida das células e consequentemente favorece o acúmulo de mutações genéticas sucessivas, contribuindo para a progressão do tumor. Além disso, a superexpressão de COX-2 está relacionada ao aumento na expressão de fatores de crescimento vascular, favorecendo a angiogênese que é considerado um mecanismo fundamental para o desenvolvimento neoplásico e a formação de metástase. A COX-2 favorece também a perda da adesão celular ao tecido de origem permitindo a mobilidade e invasão em outros tecidos. Pesquisas demonstraram que o aumento na expressão de COX-2 está relacionado ao aumento na atividade de determinadas proteínas, como as metaloproteinases, enzimas responsáveis pela digestão do colágeno na matriz intercelular, permitindo o rompimento das barreiras e invasão tecidual.
A alta expressão de COX-2, e a consequente produção de prostaglandinas, está associada a diminuição da resposta imune em neoplasias. Atualmente, um dos focos de pesquisa oncológica é a participação das células T reguladoras (Treg) no desenvolvimento tumoral, uma vez que estas células modulam negativamente a resposta antitumoral do organismo frente às neoplasias.
EXPRESSÃO DE COX 2 COMO FATOR PROGNÓSTICO E PREDITIVO
Em oncologia há uma busca constante de fatores prognósticos e preditivos que possam auxiliar na escolha de terapias e na previsão do comportamento das neoplasias. Sendo assim é definido como fator prognóstico qualquer característica do paciente ou do tumor que pode ser usado para prever a evolução da doença. A alta expressão de COX-2 avaliada principalmente por imunoistoquímica tem sido relacionada a tumores de comportamento agressivo conforme vários estudos publicados com neoplasias em cães e gatos. Atualmente a avaliação de COX-2 faz parte dos painéis imunoistoquímicos prognósticos na medicina veterinária em alguns tumores como neoplasias mamárias e melanomas.
Além da importância como fator prognóstico, a expressão de COX-2 pode ser utilizada como fator preditivo que por definição seriam as características que distinguem os pacientes que responderão a determinada terapia, a exemplo do que ocorre com a resposta aos AINES em neoplasias com alta expressão de COX-2. A seguir vamos discutir a importância da avaliação de COX-2 como fator prognóstico e preditivo em vários tumores comuns na rotina oncológica de cães e gatos.
USO DE INIBIDORES DE COX-2 NO TRATAMENTO ONCOLÓGICO
Estudos in vivo em humanos e cães com vários tipos de tumores, incluindo o carcinoma de células de transição de bexiga, carcinoma prostático, carcinoma de células escamosas, carcinomas mamários, carcinomas nasais e melanoma oral mostram benefícios com o uso de inibidores de COX-2 conforme tabela 1.
Carcinoma de células de transição de bexiga
Os carcinomas de células de transição também denominados carcinomas uroteliais são considerados os principais tumores de bexiga em cães e normalmente se originam no trígono vesical, tornando a remoção cirúrgica um desafio clínico muitas vezes associado a taxas altas de complicações. Por isso a busca de terapias paliativas que controlem o crescimento do tumor e melhorem os sinais clínicos relacionados à doença são objetivos comuns no tratamento de carcinomas de bexiga.
Atualmente os carcinomas uroteliais são considerados os principais modelos de estudo da expressão de COX-2 em câncer na medicina veterinária devido à alta expressão desse marcador e dos benefícios já comprovados do uso de AINES no tratamento dessa neoplasia.
Mohammed et al. 2002, avaliaram os efeitos dos inibidores de COX-2 na apoptose e angiogênese em cães com carcinoma de células de transição de bexiga. Dos 18 cães com tumor que receberam inibidor de COX-2, nenhum obteve remissão completa, porém 33% obtiveram remissão parcial (decréscimo em 50% do tamanho do tumor e ausência de novas lesões), 50% mantiveram a doença estável (alteração menor que 50% no volume tumoral e ausência de novas lesões) e apenas 17% apresentaram progressão da lesão (aumento de 50% no volume tumoral ou aparecimento de novas lesões).
Knapp et al. (25) avaliaram a eficácia da combinação entre cisplatina e firocoxibe em cães com o mesmo tipo de tumor de bexiga, comparando com o uso da cisplatina isolada. A taxa de remissão do grupo de cães que utilizou a combinação dos fármacos foi de 57%, enquanto que os pacientes que fizeram uso da cisplatina de forma isolada obtiveram uma taxa de resposta de apenas 13%. Os autores ainda salientam que os animais que fizeram uso do firocoxibe de forma isolada apresentaram remissão parcial ou doença estável em 20 e 33% dos casos, respectivamente. Os resultados deste trabalham demostram a eficácia do uso do firocoxibe no tratamento do carcinoma de células de transição de bexiga em cães associado a quimioterapia, ou de forma isolada durante o tratamento paliativo.
Carcinoma de próstata
Os carcinomas prostáticos em cães são menos comuns quando comparados a seres humanos, porém devido à evolução silenciosa e rápida normalmente são diagnosticados em estágios avançados, com presença de metástase no momento do diagnóstico, tornando a busca por terapias paliativas que controlem o crescimento do tumor o foco do tratamento. Sorenmo et al. (2004) avaliaram a expressão de COX-2 em carcinomas prostáticos caninos e observaram que 88,2% dos casos apresentavam expressão e que os cães que fizeram uso de AINE tiveram aumento de sobrevida em relação ao grupo não tratado (6,9 meses e 0,9 meses respectivamente) demonstrando mais uma vez o benefício dessa modalidade terapêutica no tratamento oncológico.
Carcinomas nasais
Os carcinomas nasais correspondem a dois terços das neoplasias de seios nasais em cães e apresentam comportamento invasivo e atualmente são tratados com radioterapia como modalidade padrão.

Figura 2 – Cão, Labrador, F com deformidade facial secundária a carcinoma nasal.
Um estudo verificou a associação de radioterapia com firocoxibe em relação ao uso de radioterapia com placebo em 24 cães com carcinomas nasais. O tempo livre de doença e sobrevida do grupo tratado com firocoxibe foi de 228 e 335 dias respectivamente enquanto que o grupo que recebeu apenas radioterapia, essas variáveis foram de 234 e 244 dias respectivamente. Apesar de não haver diferença estatística significativa entre os dois grupos, os cães que receberam AINE tiveram aumento na qualidade de vida, segundo questionário respondido pelos tutores, com melhora do apetite e atividade física dos animais, confirmando o benefício clínico do uso de firocoxibe para esses pacientes, uma vez que para tumores inoperáveis como no caso de carcinomas de seios nasais, a manutenção da qualidade de vida dos pacientes é a meta principal durante o tratamento paliativo.
Carcinomas mamários
As neoplasias mamárias em cadelas e gatas são extremamente comuns na rotina oncológica, sendo os carcinomas mamários o grupo mais frequente entre as neoplasias malignas. A remoção cirúrgica é o tratamento de escolha, porém pacientes com subtipos histológicos agressivos, estadiamento clínico avançado ou alto grau histológico podem se beneficiar do tratamento sistêmico adjuvante com quimioterapia e/ou inibidores de COX-2. Diversos estudos correlacionaram a imunomarcação de COX-2 em carcinomas mamários com agressividade tumoral e menor sobrevida das pacientes, tornando um importante fator prognóstico nesses casos, além de ser um fator preditivo, pois animais com alta expressão de COX-2 no exame de imunoistoquímica são candidatos à terapia com AINE.
Lavalle et al. (2012) avaliaram o uso de quimioterapia associada ou não a AINE em pacientes submetidas a mastectomia para tratamento de carcinomas mamários agressivos em comparação a pacientes que foram submetidas apenas a modalidade cirúrgica e observaram aumento de sobrevida nas cadelas que fizeram o uso de tratamento sistêmico. Outro resultado importante desse estudo, é que não foram relatados efeitos adversos graves com o uso prolongado de firocoxibe, demonstrando a segurança desse fármaco para regimes prolongados de administração.
Além do uso dos AINES pós mastectomia em carcinomas mamários agressivos, alguns autores avaliaram a expressão de COX-2 e a resposta a terapia com inibidores de COX-2 em carcinomas inflamatórios mamários de cadelas, que é considerada uma apresentação clínica de carcinomas mamários com invasão linfática dos vasos da derme, caracterizada por dor, edema de membros, alto potencial de metástase em que devido ao quadro avançado, as pacientes não são candidatas a remoção cirúrgica, tornando o tratamento paliativo a opção mais indicada na maioria dos casos.
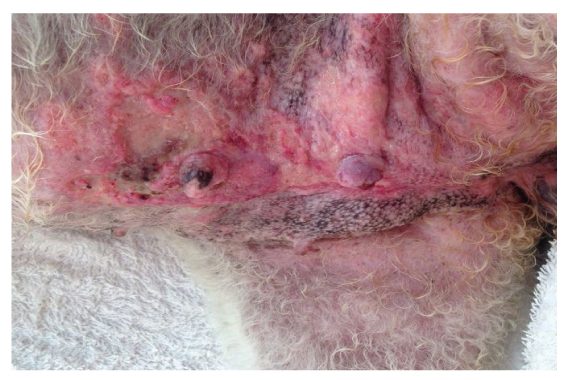
Figura 3 – Cão, F, SRD, com lesão eritematosa, em placa, com áreas de ulceração e edema local com laudo histopatológico de carcinoma micropapilar com invasão linfática dos vasos de derme, sugerindo um carcinoma inflamatório.
Todos os carcinomas inflamatórios tiveram alta expressão de COX-2 e o uso de AINE melhorou a qualidade de vida dos pacientes e manteve a doença estável por um período superior aos protocolos quimioterápicos.
Carcinomas espinocelulares
Carcinomas espinocelulares (CEC) em cães apresentam prognósticos distintos de acordo com a localização anatômica dos mesmos, sendo os cutâneos relacionados à alta invasão local, porém baixa taxa de metástase, enquanto que nos CEC orais, os tonsilares, apresentam maiores taxas de metástase quando comparados a CEC em outras localizações da cavidade oral.
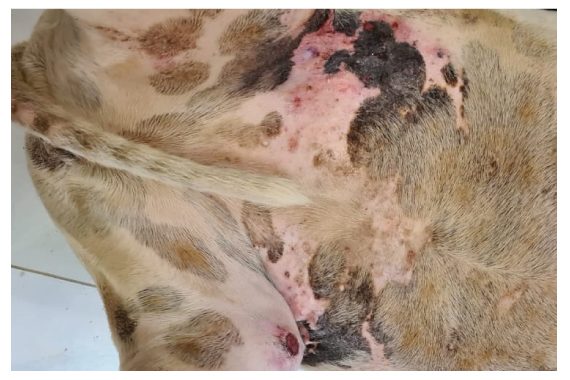
Figura 4 – Cão, Pitbull, F com lesões eritematosas secundárias a dermatite actínica e áreas de carcinoma espinocelular cutâneo.
Os CEC cutâneos têm alta correlação com exposição solar e alguns estudos sugerem que já nas lesões pré -neoplásicas como dermatites actínicas há expressão de COX-2, tornando possível a hipótese do benefício do uso de AINES nesses pacientes. Albanese et al. (2013) demonstraram que 4/5 cães com dermatite actínica tratados com firocoxibe durante 6 meses apresentaram melhora clínica significativa, além de alterações no exame histopatológico antes e após o início da terapia, sugerindo que a COX-2 é necessária para a síntese de prostaglandinas que estimulam a proliferação de queratinócitos e que o uso de firocoxibe pode ter um efeito antiproliferativo benéfico nessas situações.
Em relação aos CEC de cavidade oral, Schmidt et al. 2001 (26) avaliaram o uso de AINE em carcinomas de células escamosas de cavidade oral em cães o observaram que as taxas de resposta são similares aquelas utilizando drogas citotóxicas, sugerindo desta forma a eficácia dos inibidores de COX-2 no tratamento desta neoplasia.
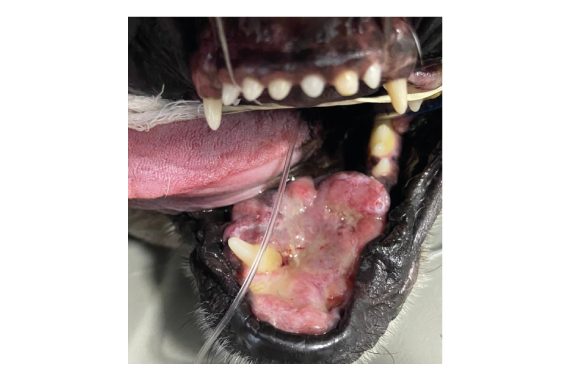
Figura 5 – Cão, F, Pug, 11 anos com lesão ulcerada em região rostral de mandíbula com laudo histopatológico de carcinoma espinocelular.
Melanoma
Os melanomas em cães possuem prognóstico dependente da localização sendo que os cutâneos apresentam menores taxas de metástase e, portanto prognósticos mais favoráveis em relação aos orais. Em um estudo avaliando a expressão de COX-2 em tumores melanocíticos foi observado que todos os melanomas orais apresentaram positividade alta e intensa no exame de imunoistoquimica, sugerindo que a inibição de COX-2 pode ser benéfica nesses pacientes.
Embora ainda não existam estudos em larga escala sobre o assunto, pesquisas in vitro demonstraram redução na proliferação e aumento da apoptose de linhagens de células de melanoma tratadas com AINE, sugerindo potencial benefício dessa terapia no tratamento de melanomas.
NEOPLASIA |
RESULTADOS |
AUTORES |
|---|---|---|
Carcinoma de bexiga | Firocoxibe associado a quimioterapia resultou | Knapp et al. 2013 |
Carcinoma prostático | Cães que fizeram uso de AINE tiveram aumento | Sorenmo et al. 2004 |
Carcinoma nasal | O tempo livre de doença e sobrevida do grupo | Cancedda et al. 2015 |
Carcinomas mamários | Pacientes submetidos a quimioterapia associada | Lavalle et al. 2012 |
Carcinomas mamários | Todos os carcinomas inflamatórios tiveram alta | Souza et al. 2009 |
Carcinoma espinocelular oral | Pacientes que fizeram o uso de AINE tiveram | Schmidt et al. 2001 |
Dermatite actínica e | 4/5 cães com dermatite actínica tratados com | Albanese et al. 2005 |
Melanomas | Pesquisas in vitro demonstraram redução na | Seo et al. 2014 |
Tabela 1 – Uso de AINES no tratamento de neoplasias em cães
USO DE ANTIINFLAMATÓRIOS NO CONTROLE DA DOR EM PACIENTES ONCOLÓGICOS
Além do uso direcionado para o controle do crescimento de certos tipos de neoplasia que expressam COX-2, os AINEs podem ser aliados para o controle de dor em certas situações na oncologia veterinária. A inibição de COX-2 bloqueia a formação de prostaglandinas que apresentam função de sensibilizar nociceptores periféricos terminais que produzem dor localizada e hipersensibilidade. Além da percepção de dor periférica, a COX-2 media a formação de prostaglandinas envolvidas na dor central, sendo que o uso de AINEs pode ser um importante auxiliar no controle de dor nessas situações.
Casos oncológicos que apresentam nível de dor elevado como, por exemplo, quadros que envolvem lise óssea como osteossarcomas ou outros tumores com invasão óssea secundária como carcinomas com metástase óssea, tumores nasais com destruição óssea secundária, neoplasias orais com infiltrado ósseo ou neoplasias com infiltrados inflamatórios extensos, que sabidamente apresentam nível elevado de dor, podem se beneficiar do uso de AINES como o firocoxibe.
Outra aplicação do uso dos inibidores de COX-2 refere-se a dor pós-operatória em cirurgias oncológicas como, por exemplo, mastectomias, cirurgias cutâneas reconstrutivas, cirurgias ortopédicas oncológicas, cirurgias abdominais ou torácicas para remoção de neoplasias.
MONITORAMENTO DE EFEITOS ADVERSOS DURANTE O USO DOS INIBIDORES DE COX-2
Pacientes oncológicos que fazem uso de AINE seja direcionado contra o crescimento tumoral ou no auxilio ao controle de dor apresentam como característica principal a necessidade do uso crônico desses fármacos, portanto a escolha do tipo de inibidor de COX-2 deve ser pautada em fármacos que sejam seguros em longo prazo.
O firocoxibe é uma opção que atende esses critérios, pois estudos em cães saudáveis submetidos à terapia com firocoxibe oral por 30 dias nas doses convencionais não demonstraram alterações em variáveis do hemograma, exame bioquímico, avaliação de sangue oculto nas fezes ou alteração endoscópica sugerindo que esse fármaco é seguro para uso crônico em cães, desde que respeitado os critérios de seleção dos pacientes.
Apesar do firocoxibe ser um fármaco seguro para uso crônico, o monitoramento de efeitos adversos principalmente gastrointestinais e renais deve ser obrigatório nesses pacientes com o intuito de prevenir ou manejar possíveis alterações decorrentes da terapia. Portanto é obrigatório que animais submetidos à terapia com AINE sejam avaliados antes de iniciar o tratamento, através de história clínica, exame físico e exames hematológicos de hemograma, função hepática, função renal, urinálise e que esses mesmos exames sejam realizados periodicamente durante a terapia a fim de monitorar possíveis alterações decorrentes do uso da terapia. Além disso, os tutores devem ser orientados a monitorar e reportar efeitos adversos como êmese, diarreia, hiporexia/anorexia e interromper a administração e contatar o médico veterinário responsável pelo caso nessas situações. Outro ponto importante a ser considerado é evitar o uso em pacientes desidratados, com doenças renais ou hepáticas prévias, ou em animais que fazem uso de diuréticos ou corticoides que podem agravar de forma substancial os efeitos adversos oriundos dessa terapia.
Considerações finais
A relação da expressão de COX-2 com a carcinogênese está bem descrita em diversas neoplasias tanto em humanos como em animais. O uso de inibidores de COX-2 como o firocoxibe, no tratamento de tumores que expressam a COX-2 demonstraram resultados promissores enfatizando uma modalidade terapêutica adjuvante.
Referência Bibliográfica
AUTOR

Dr. Paulo César Jark
Médico Veterinário pela Universidade do Estado de Santa Catarina – UDESC
Residência em Clínica Médica de Pequenos Animais – UNESP Botucatu
Especialização em Oncologia Veterinária pelo Instituto Bioethicus- Botucatu
Mestrado e Doutorado em Clínica Médica com enfoque em Oncologia Veterinária pela UNESP Jaboticabal
Realizou programa de Doutorado no exterior na University of Madison Wisconsin – EUA
Vice presidente da Sociedade Latinoamericana de Oncologia Veterinária- SLOVET
Professor colaborador do Programa de Pós-graduação da Unesp Jaboticabal
Coordenador da ONCONNECTIONVET e ONCCAREVET
Compartilhe esta matéria!
#botupharmapet #petlovers #cães
Inscreva-se para receber novidades e concorra a um brinde especial todo mês
As cicloxigenases (COX) são enzimas responsáveis pela cicloxigenação e peroxidação do ácido araquidônico presente na membrana celular, levando a formação de prostaglandinas.
As cicloxigenases (COX) são enzimas responsáveis pela cicloxigenação e peroxidação do ácido araquidônico presente na membrana celular, levando a formação de prostaglandinas.